Mehr Erfolg durch Interdisziplinarität
Dr. med. Marvin Lucas Biller, Dr. med. univ. Klemens Paul Kaiser, Dr. med. Elena Plawetzki, Dr. med. Julian Bucur, Univ.-Prof. Dr. med. Thomas Kohnen
Zusammenfassung
Durch mikro- und makroangiopathische Veränderungen können im Rahmen der Erkrankung Schäden an verschiedenen Organsystemen auftreten, die vor allem das Herz-Kreislauf-System, die Nieren, die Nerven und die Sehorgane betreffen. Das Management des Diabetes mellitus stellt deshalb eine interdisziplinäre Herausforderung dar, die einen fachübergreifenden Austausch über die diagnostischen und therapeutischen Modalitäten der jeweiligen Fachdisziplinen erfordert.
In der Augenheilkunde sind es insbesondere die diabetische Retinopathie und Makulopathie, die im Rahmen des Diabetes auftreten können und frühzeitig erkannt und behandelt werden müssen. Dabei werden diabetische Netzhautveränderungen trotz großer Fortschritte sowohl in der Diagnostik als auch der Therapie fatalerweise noch immer oft zu spät erkannt, was die Prognose sowohl für die Sehkraft als auch die Lebensqualität der Betroffenen deutlich einschränkt [1]. In diesem Beitrag sollen die Grundlagen der augenärztlichen Versorgung von Patienten mit Diabetes mellitus aufgezeigt und diskutiert werden.
Fortbildungsziele
- Welche Patientengruppen sind besonders von einem Sehverlust durch ihre Diabeteserkrankung bedroht?
- Wie und in welchen Abständen laufen augenärztliche Verlaufskontrollen bei Diabetes mellitus ab?
- Wie kann man diabetische Veränderungen der Netzhaut einteilen und erkennen?
- Welche Therapiemöglichkeiten stehen zur Verfügung und welche Chancen und Risiken bergen diese?
Einleitung
Unter der diabetischen Retinopathie und Makulopathie versteht man mikroangiopathische Komplikationen des Diabetes mellitus, welche die Netzhaut betreffen [2]. Dabei kann jede Form des Diabetes mellitus prinzipiell auch zu einer diabetischen Retinopathie oder Makulopathie führen, wobei gezeigt werden konnte, dass Typ-1-Diabetiker hinsichtlich beider Entitäten statistisch häufiger betroffen sind als die epidemiologisch größere Gruppe der Typ-2-Diabetiker [2, 3]. Insgesamt stellt die diabetische Netzhautveränderung die häufigste Ursache für Sehverlust und Erblindung in der Bevölkerung im Alter zwischen 20 und 74 Jahren in Europa und Nordamerika dar, weshalb ihr auch weitreichende gesundheitsökonomische Implikationen zukommen [4, 5]. Es sind große interdisziplinäre Anstrengungen vonnöten, um dem komplexen Krankheitsbild des Diabetes mellitus präventiv, diagnostisch und therapeutisch gerecht zu werden. Deshalb ist es für die verschiedenen am Management des Diabetes mellitus beteiligten Facharztgruppen essenziell, über weitreichende Kenntnisse der verschiedenen diagnostischen und therapeutischen Aspekte dieser Volkskrankheit zu verfügen und angesichts zahlreicher Neuerungen stets auf dem aktuellen Stand zu bleiben.
Die International Diabetes Federation (IDF) schätzte 2019 die weltweit an Diabetes mellitus erkrankte Population auf etwa 463 Millionen Menschen mit einer prognostizierten Zunahme auf etwa 700 Millionen Menschen bis zum Jahr 2045 [6]. Die Prävalenz des diagnostizierten Diabetes mellitus in Deutschland stieg unter allen Versicherten der AOK Hessen dabei zwischen 2000 und 2009 um 3,2 % auf 9,7 % an [7]. Dabei ergab eine Studie, die im nahgelegenen Mainz und Umgebung im Jahr 2015 mit etwa 15.000 Teilnehmer durchgeführt wurde, dass etwa 20 % aller Diabetiker von einer diabetischen Retinopathie betroffen sind [8]. Etwa 5 % aller identifizierten Diabetiker der Studie seien dabei bereits von einer Verschlechterung der Sehleistung bedroht. Insgesamt schlussfolgerten die Autoren anhand von Hochrechnungen, dass etwa 140.000 Menschen in Deutschland zwischen 35 und 74 Jahren zukünftig Gefahr liefen, an den Folgen einer diabetischen Retinopthie zu erblinden.
Risikofaktoren, die mit der Entwicklung und Progression diabetischer Netzhautveränderungen assoziiert sind, sind insbesondere die Dauer der Diabeteserkrankung, ein dauerhaft erhöhter HbA1c-Wert (Hyperglykämie), eine Dyslipidämie sowie das simultane Vorhandensein einer arteriellen Hypertonie und/oder einer diabetischen Nephropathie [9]. Darüber hinaus konnte Nikotinkonsum als Risikofaktor für die Entwicklung einer diabetischen Retinopathie bei Typ-1-Diabetikern identifiziert werden [10]. Im Umkehrschluss zeigte sich außerdem, dass das kardiovaskuläre Risiko bei Vorliegen einer diabetischen Retinopathie sowohl bei Typ-1- als auch Typ-2-Diabetikern deutlich erhöht ist [11]. Außerdem gelten stark schwankende Glukosewerte (was z. B. auch nach einer bariatrischen Operation auftreten kann) und eine Schwangerschaft als weitere Risikofaktoren [12].
Neben den genannten diabetogenen Netzhautschäden kann sich ein schlecht eingestellter Diabetes am Auge auch in Form von Refraktionsänderungen zeigen, da stark schwankende Blutzuckerwerte zu einem osmotischen Aufquellen der Augenlinse führen können. Dabei beschreiben die Patienten häufig sich schnell und wiederholt ändernde Brillen- oder Kontaktlinsenwerte. Außerdem kann ein Diabetes, auch bei jüngeren Patienten, die Entwicklung eines grauen Stars verursachen oder beschleunigen. Im Rahmen einer diabetischen Neuropathie kann der Nervus opticus betroffen sein, wodurch es unabhängig von einer diabetischen Retinopathie oder Makulopathie zu einer Sehveränderung oder Sehverschlechterung kommen kann. Zudem kann bei einer diabetischen Retinopathie durch Gefäßneubildungen im Auge die Zirkulation des Kammerwassers beeinträchtigt werden, was zu einer Erhöhung des Augendrucks und einem konsekutiven Sehnervenschaden (Neovaskularisationsglaukom) führen kann. Weiterhin treten makrovaskuläre Komplikationen wie embolische Ereignisse am Auge (wie ein Zentralarterienverschluss) bei Diabetes mellitus häufiger auf, was sekundär im Einzelfall ebenfalls zu weitreichenden und dauerhaften Sehschäden führen kann [13].
Interdisziplinäre Behandlung des Diabetes mellitus
Disease-Management-Programme (DMP) wurden entwickelt, um ein strukturiertes Behandlungsprogramm unter Einschluss verschiedener ärztlicher Facharztgruppen für chronisch Erkrankte zur Verfügung zu stellen. Dabei zeigt eine Studie aus Nordrhein-Westfalen, dass nur 66,7 % aller in einem DMP für Diabetes dokumentierten Patienten ihre Netzhaut regelmäßig gemäß aktuellen Empfehlungen der Fachgesellschaften untersuchen lassen. Angestrebt werden jedoch mindestens 90 % [14]. Demzufolge sollte eine enge Zusammenarbeit und Kommunikation zwischen Augenärzten und insbesondere den internistischen Facharztgruppen erfolgen, um diese Raten dauerhaft zu erhöhen.
In der aktuellen Nationalen Versorgungsleitlinie Diabetes Typ-2 [15] (zuletzt aktualisiert im Mai 2023) und der zuvor gültigen und teils übernommenen Nationalen Versorgungsleitlinie zur Prävention und Therapie von Netzhautkomplikationen bei Diabetes [12] wird ein Muster für die interdisziplinäre Zusammenarbeit zur Optimierung der Behandlung und Prävention diabetischer Netzhautveränderungen dargestellt (siehe Abb. 1).
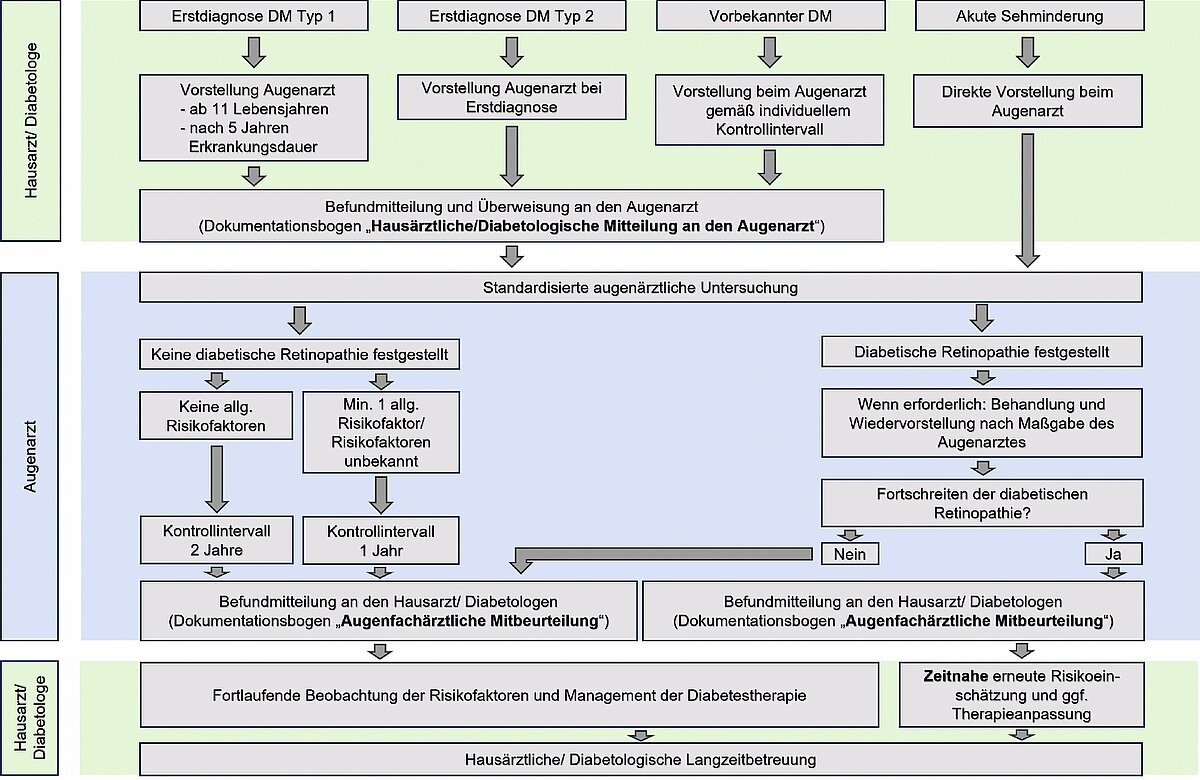
Die empfohlenen Kontrollintervalle orientieren sich dabei insbesondere am individuellen Risikoprofil eines jeden Patienten, wobei dieses dem augenärztlichen Kollegen bzw. Kollegin durch den behandelnden Internisten adäquat mitgeteilt werden sollte. Die zu diesem Zweck ausgearbeiteten Untersuchungsbögen, die eine optimierte Kommunikation vereinfachen und standardisieren sollen, werden in der klinischen Praxis jedoch noch immer relativ selten verwendet. Auch die von der Deutschen Ophthalmologischen Gesellschaft (DOG) und dem Berufsverband der Augenärzte Deutschlands (BVA) herausgegebenen Leitlinien zur diabetischen Retinopathie empfehlen die Anwendung derartiger Kommunikationsbögen [16]. Insgesamt soll durch ein derartig optimiertes interdisziplinäres Prozedere das Risiko für Diabetes-assoziierte Sehschäden minimiert werden. Gleichzeitig können progrediente diabetogene Veränderungen der Augen bzw. Netzhaut Hinweise auf eine insuffizient eingestellte Stoffwechsellage geben, was eine zeitnahe Reevaluation der Therapie und ggf. weitere Diagnostik durch den behandelnden Internisten erforderlich machen würde.
Einteilung und Pathophysiologie der diabetischen Netzhaut- komplikationen
Die diabetische Retinopathie wird in eine nicht-proliferative (NPDRP) und proliferative Form (PDRP) unterteilt. Im Vordergrund stehen bei allen Formen Veränderungen der Netzhautgefäße. Die milde nicht-proliferative diabetische Retinopathie präsentiert sich mit aneurysmatischen Ausbuchtungen der retinalen arteriellen Gefäße (sog. Mikroaneurysmen), die typischerweise asymptomatisch sind. Im weiteren progredienten Verlauf kann es durch Leckagen der retinalen Kapillaren zu intraretinalen Blutungen (moderate und schwere NPDRP) oder verschlussbedingt zu retinalen Ischämien mit Sauerstoffmangelzuständen kommen, in deren Folge eine NPDRP durch die Produktion von vascular endothelial growth-factor (VEGF) in eine PDRP übergehen kann [17]. Diese proliferative Form ist durch das Vorliegen von Neovaskularisationen charakterisiert, welche sowohl im Bereich der Netzhaut (und des Sehnerven) als auch der Regenbogenhaut (Rubeosis iridis) am vorderen Augenabschnitt auftreten können. Dies ist zusätzlich häufig mit der Formation von fibrösem Gewebe vergesellschaftet, das durch Kontraktion zu Blutungen oder einer traktionsbedingten Netzhautablösung führen kann.
Die pathologische Hochregulierung von VEGF beeinflusst nicht nur den Schweregrad der proliferativen Form, sondern steht auch in starker Korrelation mit der Entwicklung und der Ausprägung eines diabetischen Makulaödems (DMÖ). Das DMÖ, welches prinzipiell in jedem Stadium der diabetischen Retinopathie auftreten kann, ist für einen Großteil der Visusverluste bei Diabetikern verantwortlich [18]. Als pathophysiologisches Korrelat gelten Permeabilitätsstörungen und Okklusionen von Kapillaren der Makula, welche dort zu Flüssigkeitseinlagerungen führen. Typischerweise äußern sich diese durch eine Visusminderung, Schwierigkeiten beim Lesen, Metamorphopsien („Verzerrtes Sehen“) und zentrale Gesichtsfelddefekte. Außerdem können im Rahmen des Diabetes retinale mikroangiopathische Durchblutungsstörungen der Makula auftreten, wobei man von einer ischämischen Makulopathie spricht.
Diagnostik
Wie bereits zuvor erläutert, sollten bei Diabetes regelmäßige standardisierte augenärztliche Untersuchungen erfolgen. Dies umfasst unter anderem eine Visusbestimmung, die Messung des intraokularen Drucks sowie eine Untersuchung aller Augenabschnitte mithilfe der Spaltlampen-Biomikroskopie (Abb. 2).
Die Beurteilung des vorderen Augenabschnittes umfasst in der Regel insbesondere eine Begutachtung des Linsenstatus sowie der Regenbogenhaut (Iris), da sich dort ebenfalls Neovaskularisationen bilden können (Rubeosis iridis). Ebenfalls kann auch die Anwendung eines Kontaktglases (Gonioskop) zum Einsatz kommen, da beginnende Neovaskularisationen im Kammerwinkel oft übersehen werden [19].
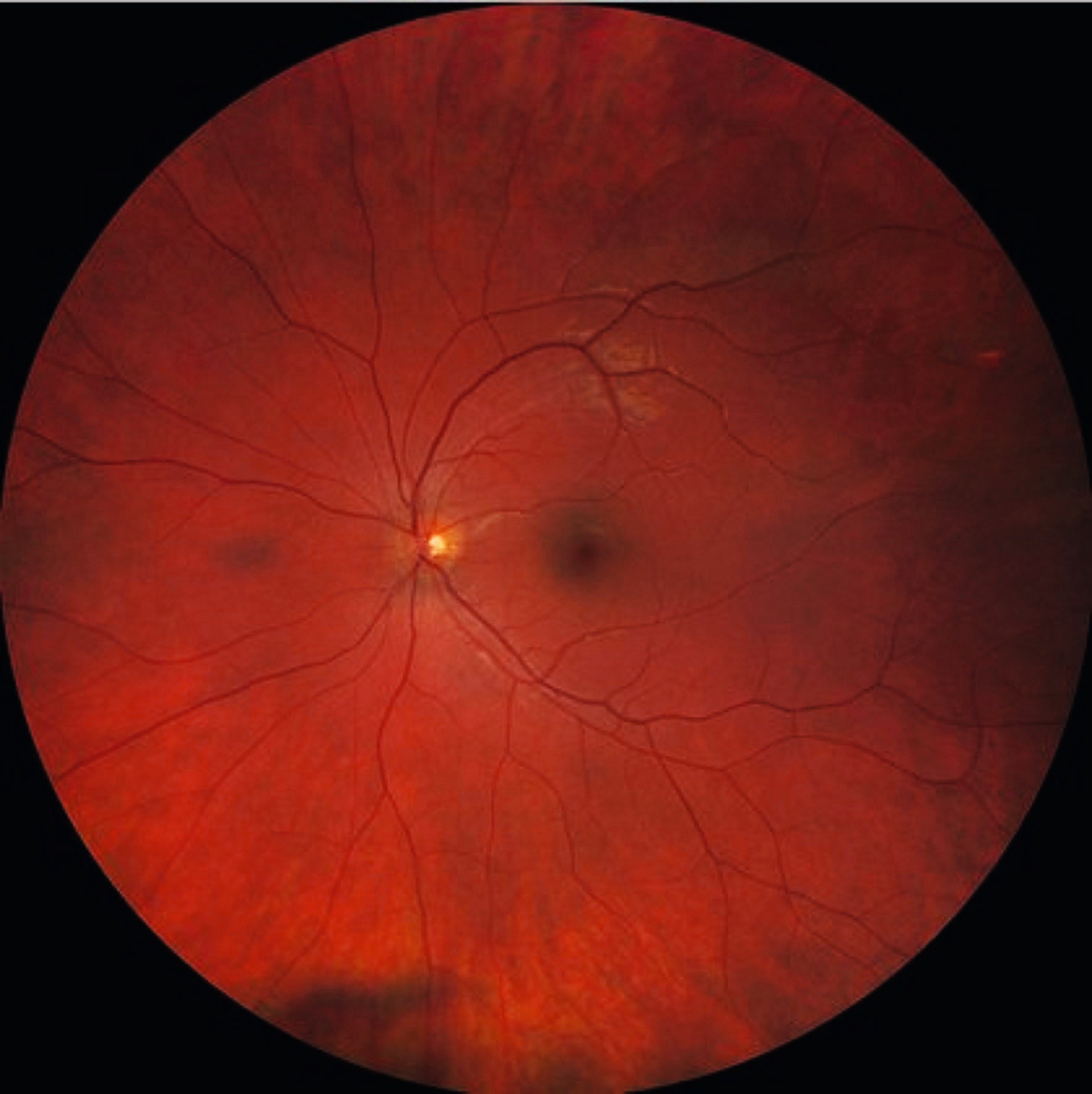
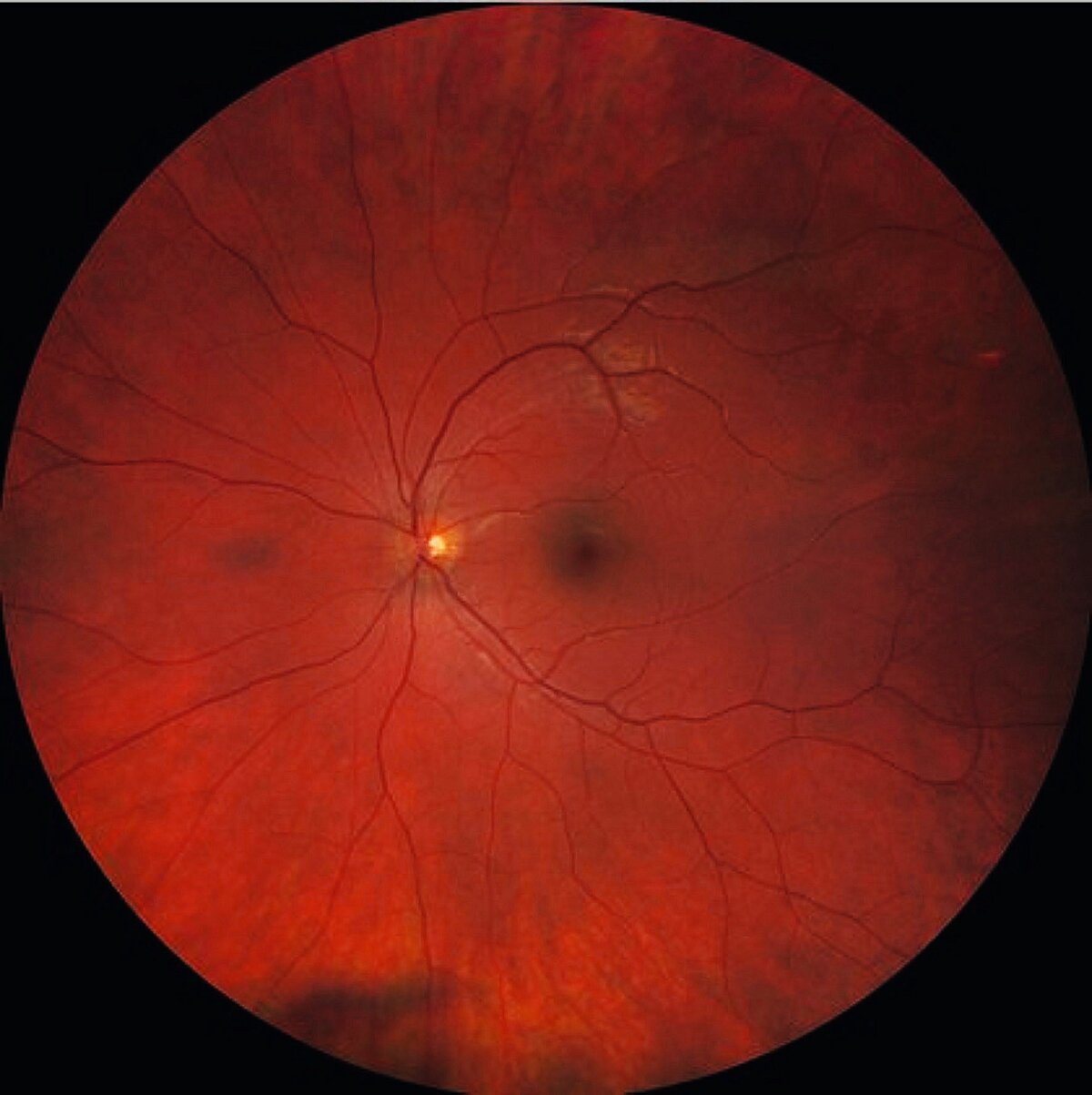
Die weiteren Untersuchungen des hinteren Augenabschnittes sollten daraufhin bei dilatierter Pupille erfolgen, um die peripheren Areale der Netzhaut adäquat einsehen zu können. Im Rahmen der Funduskopie können pathologische Veränderungen der Retina (wie z. B. Gefäßveränderungen, Blutungen, Exsudate oder eine Ödembildung) diagnostiziert und dokumentiert werden (siehe Abb. 3a).
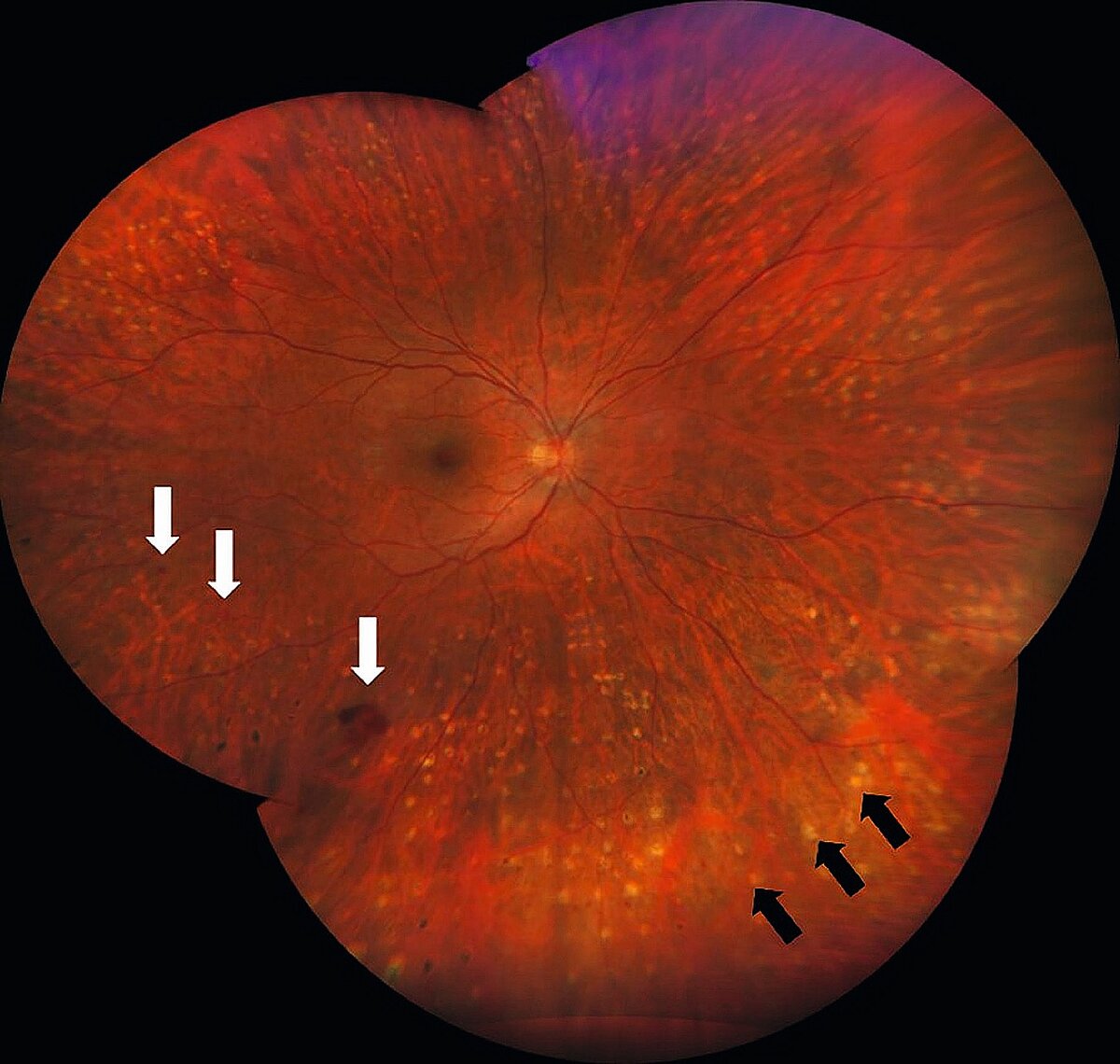
Im Vorfeld der Untersuchung ist es notwendig, die Patienten (wegen der diagnostischen Mydriasis) auf eine für den Rest des Untersuchungstags anhaltende Fahruntauglichkeit hinzuweisen. Zur Detektion von ischämischen Netzhautarealen sowie zur Darstellung von Proliferationen und Gefäßleckagen eignet sich eine Farbstoffuntersuchung der Netzhautgefäße, die sogenannte Fluoreszenzangiographie (siehe Abb. 4).

Diese erfordert den Einsatz einer speziellen Funduskamera, wobei weißes Licht durch einen blauen Anregungsfilter geleitet wird. Intravenös injizierter Fluoreszenzfarbstoff absorbiert dieses Licht, fluoresziert und emittiert Licht im gelb-grünen Spektrum, welches mithilfe eines Sperrfilters erfasst werden kann. Die Bilder werden direkt nach der Injektion nach festgelegenen Zeitpunkten aufgenommen. Mikroaneurysmen, Gefäßneubildungen sowie assoziierte Leckagen erscheinen in der Bildgebung als hyperfluoreszente Areale. Retinale Bereiche ohne Perfusion stellen sich als Hypofloureszenz dar. Zur Detektion von intra- und subretinaler Flüssigkeit sowie zur Messung der Netzhautdicke eignet sich die optische Kohärenztomographie (OCT), ein nicht-invasives diagnostisches Verfahren, das eine in-vivo Querschnittsdarstellung der Retina liefert (siehe Abb. 5). Dabei wird ein Konzept verwendet, welches als Interferometrie (Überlagerung oder Interferenz von Wellen) bekannt ist.
Damit lässt sich eine Querschnittskarte der Netzhaut mit einer Genauigkeit von etwa 10–15 µm erstellen. Das OCT wird in der Regel bei jeder Verlaufskontrolle zur Diagnostik und Beurteilung eines Makulaödems notwendig, wodurch es sich sowohl zur Indikationsstellung einer intravitrealen Therapie als auch zu deren Erfolgskontrolle eignet.
Therapie diabetischer Netzhautkomplikationen
Zentraler Bestandteil des Managements diabetischer Netzhautkomplikationen ist die Prävention. Regelmäßige augenärztliche Verlaufskontrollen und ein intensiver interdisziplinärer Austausch mit den behandelnden ärztlichen Kollegen anderer Fachrichtungen sind für die Optimierung der Visusprognose bei Diabetikern wegweisend. Sollten jedoch bereits diabetische Netzhautveränderungen vorliegen, so stehen verschiedene therapeutische Modalitäten zur Verfügung, um diese zu behandeln bzw. deren Prognose zu verbessern (siehe Tab. 1).
Tab. 1: Stadien und Therapie diabetischer Netzhautschäden (nach Hammes et al. [2]) | ||
Stadium | Ophthalmologischer Befund | Ophthalmologische Therapie |
Nichtproliferative diabetische Retinopathie (NPDRP) | ||
Milde Form | Mikroaneurysmen | Keine Laserkoagulation |
Mäßige Form | Zusätzlich einzelne retinale Blutungen, venöse Kaliberschwankungen | Keine Laserkoagulation |
Schwere Form | 4–2–1-Regel >20 einzelne Mikroaneurysmen, intraretinale Blutungen in 4 Quadranten oder perlschnurartige Venen in 2 Quadranten oder intraretinale mikrovaskuläre Anomalien (IRMA) in 1 Quadranten | Laserkoagulation nur bei Risikopatienten |
Proliferative diabetische Retinopatie (PDRP) | ||
Retinale Gefäßproliferationen (nah und fern der Papille) | Laserkoagulation, nur in ausgewählten Fällen intravitreale operative Medikamenteneingabe (IVOM) | |
Glaskörperblutung, Netzhautablösung | Laserkoagulation, wenn möglich; sonst evtl. Vitrektomie | |
Diabetische Makulopathie | ||
Diabetisches Makulaödem | Punkt-/fleckförmige Zone(n) von Ödem, intraretinalen Blutungen oder harten Exsudaten am hinteren Pol | Keine Laserkoagulation |
Wenn makulanah: klinisch signifikant (Visusbedrohend) | ||
– Ohne Beteiligung der Fovea | Gezielte Laserkoagulation | |
– Mit Beteiligung der Fovea | Intravitreale operative Medikamenteneingabe (IVOM), optional gezielte Laserkoagulation | |
Ischämische Makulopathie | Diagnose durch Fluoreszeinangiographie: Verschluss des perifovealen Kapillarnetzes | Keine Therapie möglich |
Laut aktuellen Versorgungsleitlinien kann sowohl zur Behandlung von Gefäßneubildungen im Rahmen einer proliferativen diabetischen Retinopathie als auch des diabetischen Makulaödems bei einem ausgewählten Patientenklientel die im Rahmen eines minimalinvasiven Eingriffs erfolgende Eingabe von Medikamenten in das Augeninnere erfolgen [16]. Diese gemeinhin auch als IVOM („intravitreale operative Medikamentenapplikation“) bezeichneten und ambulanten Eingriffe verwenden unter anderem Steroide und Anti-VEGF-Präparate, um die Pathomechanismen der zugrundeliegenden diabetischen Veränderungen zu durchbrechen. Die Visusuntergrenze für die Indikationsstellung der IVOM beträgt 0,05 [16)] Dadurch kann in vielen Fällen eine deutliche Verbesserung des Krankheitsbildes (Sehverbesserung) oder eine Reduktion des Fortschreitens erreicht werden. Intravitreale Injektionen werden in Deutschland durch Fachärzte für Augenheilkunde durchgeführt, welche über ausreichende Kenntnisse sowohl in der Indikationsstellung als auch der Durchführung verfügen müssen. Der Eingriff muss in hierfür nach den aktuellen Qualitätssicherungsmaßnahmen geeigneten Räumen erfolgen. Eine präoperative Aufklärung sollte insbesondere Erläuterungen über die Symptome einer postoperativen Druckerhöhung und Endophthalmitis beinhalten (vor allem Rötung, Schmerzen, Sehverschlechterung oder vermehrte Blendempfindlichkeit). Zunächst erfolgt eine topische Anästhesie durch die Instillation mehrerer Tropfen eines Lokalanästhetikums. Unter sterilen Bedingungen erfolgt der Einstich im Bereich der Pars plana etwa 3,5–4,0 mm (je nach Linsenstatus) neben dem Hornhaut-rand (siehe Abb. 7).
Direkt nach der Injektion in das Augeninnere muss die Prüfung auf Wahrnehmung von Lichtschein erfolgen, um eine mögliche akute retinale Perfusionsstörung durch einen intraokularen Druckanstieg auszuschließen (bedingt durch das injizierte Volumen des Medikaments). Je nach Applikationsmenge ist eine postoperative Augendruckkontrolle etwa 60 Minuten nach der Injektion obligat [20]. Essenziell ist die ophthalmologische Kontrolluntersuchung mittels Spaltlampenuntersuchung, Augendruckmessung und Fundusuntersuchung 1–4 Tage nach der intravitrealen Eingabe eines Medikaments, um eine möglicherweise beginnende Endophthalmitis frühzeitig entdecken zu können. Eine leichte Rötung im Bereich der Einstichstelle („Hyposphagma“) ist in der Regel ohne therapeutische Konsequenz und tritt regelhaft auf.
Hinsichtlich der Behandlungsintervalle stehen mehrere Strategien zu Verfügung. Als Grundsatz gilt jedoch „So viel wie nötig – so wenig wie möglich“. Bei dem sogenannten „pro re nata“-Schema (PRN) wird beispielsweise nach einer Dreierserie mit einem anti-VEGF-Inhibitor im Abstand von vier Wochen zunächst auf ein Pausieren der Therapie mit regelmäßigen Verlaufskontrollen abgezielt. Sollte es weiterhin oder erneut zu einer Krankheitsaktivität (z. B. Flüssigkeitsansammlung in der Netzhaut) kommen, wird die Therapie mit weiteren Injektionen fortgeführt. Bei dem sog. Treat-and-Extend-Schema (T&E) folgt nach einem initialen Injektionszyklus von bspw. drei IVOMs alle vier Wochen eine Verlängerung des Injektionsabstands zwischen den Serien um jeweils zwei Wochen, wenn die Krankheitsaktivität zurückgedrängt und ein trockener Befund stabilisiert werden konnte [21]. Der Unterschied beider Schemata besteht vor allem darin, dass beim T&E-Schema ein Ausschleichen der IVOM-Therapie erfolgt.
Bei der intravitrealen Injektion von Depotsteroiden sollten keine Behandlungsserien, sondern einzelne IVOM erfolgen. Wichtig ist hierbei die regelmäßige Kontrolle des Augeninnendrucks, da in einigen Fällen ein intraokularer Druckanstieg nach der Injektion von Depotsteroiden beobachtet wurde. Zudem kann die Eingabe von Depotsteroiden die Entwicklung einer Katarakt beschleunigen, worüber die Patienten aufgeklärt werden müssen. Nach der Eingabe von zugelassenen Dexamethasonpräparaten sollte die Reevaluierung der erneuten Eingabe nach etwa drei Monaten im Rahmen von monatlichen Kontrollen erfolgen [22]. Nach der Eingabe eines Fluocinolonimplantats wird von einer Wirkstofffreisetzung über bis zu drei Jahren ausgegangen, jedoch kann ein frühzeitiges Nachlassen der Wirkung auftreten, weswegen auch im ersten Jahr neben dem Augendruck die Wirksamkeit kontrolliert werden sollte [23].
Die Laserkoagulation der Netzhaut (kurz LK oder LAKO) stellt eine weitere seit Jahrzehnten etablierte Therapieoption einiger diabetischer Netzhautkomplikationen dar. Dabei werden mithilfe eines Argonlasers, der an eine Spaltlampe angeschlossen ist, kleine Energieherde auf der Netzhaut erzeugt, die anschließend die Bildung einer lokalen chorioretinalen Narbe induzieren. Anders als bei der LAKO von Netzhautlöchern (Foramen), die eine dauerhafte „Abriegelung“ des Defekts zur Prävention einer Netzhautablösung zum Ziel hat, beabsichtigt man mit dem Verfahren bei der proliferativen diabetischen Retinopathie eine lokale Reduktion retinaler Stoffwechselprozesse (insbesondere in ischämischen Netzhautbereichen). Dadurch können bestimmten Pathomechanismen (wie z. B. die Ausschüttung von VEGF oder proinflammatorischer Faktoren) durchbrochen werden, was lindernde Auswirkungen insbesondere auf die Ausbildung retinaler Neovaskularisationen hat.
Im Rahmen der panretinalen (peripheren) Laserkoagulation werden dabei in mehreren Sitzungen (zumeist vier) von etwa sieben bis 14 Tagen Abstand periphere Bereiche der Netzhaut mit dem Laser behandelt, wobei in einem Gittermuster oftmals insgesamt über 1.000 Herde erzeugt werden (siehe Abb. 6).
Bei dem zumeist ambulanten Eingriff nehmen die Patienten an einer Spaltlampe Platz, woraufhin (nach einer Oberflächenbetäubung der Hornhaut durch anästhesierende Augentropfen) ein Kontaktglas mit einem Kontaktgel auf das jeweilige Auge aufgesetzt wird. Durch das Setzen der Laserimpulse können drückende Schmerzen auftreten, worauf mit einer Reduktion der Laserenergie reagiert werden kann. Insgesamt setzt das Verfahren an der Spaltlampe kooperative Patienten voraus. Alternativ kann eine Laserkoagulation auch im Rahmen eines operativen Eingriffs (z. B. Pars-Plana-Vitrektomie, siehe unten) unter Einfluss invasiverer Betäubungsmethoden (wie z. B. einer Peribulbäranästhesie) oder sogar in Intubationsnarkose durchgeführt werden. Seit einigen Jahren stehen außerdem neuartige Lasersysteme zur Verfügung, welche mithilfe digitaler Navigation und ohne Kontaktglas eine effiziente und schnelle periphere Laserkoagulation der Netzhaut durchführen können (NAVILAS®) [25]. Die Laserkoagulation der peripheren Netzhaut findet sowohl bei der diabetischen Retinopathie als auch der Makulopathie Anwendung.
Beim diabetischen Makulaödem kann außerdem eine fokale Laserkoagulation des betroffenen Bereichs der Netzhaut um die Makula herum erfolgen, wobei dies jedoch nicht risikolos ist und genaustens abgewogen werden sollte.
Neben Schmerzen sollten Patienten im Rahmen der Aufklärung vor einer Laserkoagulation der Netzhaut insbesondere über die Möglichkeit von Gesichtsfelddefekten informiert werden. Zudem besteht ein Risiko für das zentrale Sehen, und auch die Nacht- und Farbwahrnehmung kann durch den Eingriff negativ beeinflusst werden.
Eine Alternative zur Laserkoagulation stellt die Kryo- bzw. Kältetherapie dar, bei welcher durch Anwendung einer etwa -70° kalten Sonde ebenfalls eine lokale Vernarbung der Netzhaut induziert wird. Dieses findet vor allem dann Anwendung, wenn eine Laserkoagulation beispielsweise aufgrund von Linsentrübungen oder einer Glaskörperblutung nicht möglich ist. Wegen der höheren Invasivität findet eine Kryokoagulation deshalb meist im Rahmen größerer stationärer vitreoretinaler Eingriffe statt (siehe unten).
Bei prolongierten Verläufen können sekundäre Krankheitsschäden entstehen, die das Sehen dauerhaft und irreversibel schädigen können. Zu diesen zählen insbesondere Glaskörperblutungen, die als Folge der Neovaskularisationen auftreten und den Lichteinfall in den Bulbus massiv behindern können. Derartige Blutungen resorbieren sich in vielen Fällen (trotz längeren Zuwartens) nicht spontan. Außerdem können fibröse Membranen im Rahmen einer proliferativen Vitreoretinopathie (PVR) (siehe Abb. 3b) Zug auf die Netzhaut ausüben und dadurch eine Netzhautablösung auslösen.

In solchen Fällen kann oft nur noch operativ im Rahmen einer Pars-Plana-Vitrektomie (PPV) behandelt werden. Dabei wird über Inzisionen im Bereich des Limbus über Sklerostomien ein instrumenteller Zugang in das Augeninnere geschaffen, über welchen verschiedene Operationsschritte (wie z. B. das Entfernen des Glaskörpers (Vitrektomie) oder eine Laserkoagulation der Netzhaut) durchgeführt werden können. Außerdem muss in besonderen Fällen (wie z. B. bei einer Netzhautablösung) eine Tamponade aus Silikonöl oder Gas in das Auge instilliert werden. Eine Öltamponade wird in den meisten Fällen nach einigen Wochen im Rahmen einer weiteren PPV entfernt und durch Luft oder Gas ersetzt, woraufhin eine besondere postoperative Lagerung (mit Blick nach unten) für einige Tage notwendig ist. Durch Fortschritte sowohl in der Operationstechnik als auch bei der verwendeten Instrumentation (z. B. durch die Einführung von weniger invasiven 23-Gauge-Systemen) ist der Eingriff heute deutlich weniger invasiv als noch vor einigen Jahrzehnten. Trotzdem bleibt eine PPV in den meisten Fällen weiterhin mit einem stationären Aufenthalt verbunden, da postoperativ neben Blutungen, Entzündungsreaktionen und Infektionen vor allem akute Veränderungen des Augendrucks auftreten können. Diese können sowohl Druckabfälle (bei Undichtigkeiten der Sklerostomien) als auch Druckerhöhungen (z. B. bei Entzündungen, anatomische Veränderungen oder Reaktionen auf intra- oder postoperativ verabreichte Medikamente) umfassen. Nach Ende des stationären Aufenthalts folgt meistens eine gemeinsame Betreuung mit dem behandelnden Augenarzt. Bei einer Stabilisierung des Befundes kann die weitere ärztliche Betreuung oft wieder vollständig durch den behandelnden Augenarzt übernommen werden.
Die Rolle künstlicher Intelligenz
Automatisierte Bilderkennungsprogramme, die auf künstlicher Intelligenz (KI) basieren, versuchen insbesondere Fundusfarbaufnahmen zu befunden, wodurch klinisch-relevante Netzhautveränderungen frühzeitig erfasst oder ausgeschlossen werden sollen. Dadurch werden einerseits Chancen für die Versorgungssicherung gesehen, andererseits jedoch auch Bedenken hinsichtlich der Zukunft etablierter Qualitätsstandards geäußert [15].
Im deutschsprachigen Raum stehen in diesem Zusammenhang vor allem Untersuchungen aus der Universitätsaugenklinik Greifswald zur Verfügung. So wurde in einer dort durchgeführten Studie ein durch die FDA zugelassenes KI-basiertes System (IDx-DR-System) zum Screening auf eine diabetische Retinopathie verwendet, wobei Fundusfotografien befundet wurden [24]. Dabei konnte bei etwa 60 % der Teilnehmer ein Fundusfoto mit hinreichender Qualität in Miosis gewonnen werden, die restlichen Aufnahmen konnten für die Analyse durch die KI nicht verwertet werden. Unter Ausschluss der nicht auswertbaren Aufnahmen lag die Sensitivität für die Erkennung einer behandlungsbedürften diabetischen Retinopathie bei 95,7 %, die Spezifität bei 89,1 %. Unter Betrachtung sämtlicher gewonnener Aufnahmen lagen Sensitivität und Spezifität bei jeweils 65,2 % und 66,7 % [15, 24]. Außerdem zeigte sich, dass das KI-basierte System den Schweregrad der diabetischen Retinopathie deutlich häufiger überschätzt als unterschätzt [24]. Einschränkend sollte zu dieser Studie gesagt werden, dass das untersuchte Kollektiv jünger war als die in DMP-Programmen eingeschlossenen Patienten in Deutschland und die Untersuchungen in einer diabetologischen Schwerpunktklinik stattfanden [15].
Da die meisten KI-basierten Systeme Fundusfotografien in Miosis verwenden, wird in ihrer Verwendung vor allem ein Potenzial für die Herabsetzung der Barrieren im Retinopathie-Screening gesehen, da die Verfügbarkeit von Augenärzten (vor allem in ländlichen Gebieten) gering ist und viele Patienten das Weitstellen der Pupille als lästig empfinden. Außerdem könnten Chancen in der Entlastung des augenärztlichen Personals (z. B. durch KI-unterstützte Verlaufsbeurteilungen oder besserer Darstellbarkeit gegenüber dem Patienten) liegen. Dabei ist jedoch weiterhin zu beachten, dass in Miosis oftmals keine adäquaten Fotografien der Netzhaut möglich (vor allem bei fortgeschrittenen Linsentrübungen) und periphere Netzhautveränderungen nicht erfassbar sind [15, 24]. Außerdem gilt es zu klären, ob auch andere Gruppen der Krankenversorgung (wie z. B. Optiker oder Apotheken) derartige KI-basierte Untersuchungen anbieten können und wer in solchen Fällen juristisch für die erstellten Befunde haftet. In der aktuellen Nationalen Versorgungsleitlinie Diabetes Typ-2 wird ein derartiger nicht-ärztlicher Einsatz KI-basierter Systeme beim Retinopathiescreening aufgrund der mangelnden Überprüfbarkeit und Erläuterung der Befunde kritisch gesehen [15]. Außerdem wird ein Zertifizierungssystem angeregt, um einen Qualitätsstandard bezüglich der verwendeten Kameras, der Software (und ihrer Updates), der Räumlichkeiten und der Qualifikationen des involvierten Personals zu etablieren [15].
Fazit für die Praxis
Diabetespatienten …
… müssen interdisziplinär ärztlich betreut werden.
… benötigen regelmäßige augenärztliche Verlaufskontrollen.
… benötigen eine stadiengerechte Diagnostik und Therapie.
… müssen über ihre Erblindungsgefahr aufgeklärt werden.
Dr. med. Marvin Lucas Biller
Dr. med. univ. Klemens Paul Kaiser
Dr. med. Elena Plawetzki
Dr. med. Julian Bucur
Univ.-Prof. Dr. med. Thomas Kohnen
Klinik für Augenheilkunde, Goethe-Universität Frankfurt am Main, Theodor-Stern-Kai 7, 60590 Frankfurt, Korrespondenz per E-Mail: MarvinLucas.Biller@kgu.de
Die Literaturhinweise finden Sie hier.
Multiple Choice-Fragen
Die Multiple Choice-Fragen zu dem Artikel „Diabetische Retinopathie“ von Univ.-Prof. Dr. med. Thomas Kohnen et al. finden Sie im Portal (https://portal.laekh.de) sowie in der PDF-Version dieses Artikels. Die Teilnahme zur Erlangung von Fortbildungspunkten ist ausschließlich online über das Mitglieder-Portal vom 25. Februar bis 24. August 2024 möglich. Die Fortbildung ist mit drei Punkten zertifiziert. Mit Absenden des Fragebogens bestätigen Sie, dass Sie dieses CME-Modul nicht bereits an anderer Stelle absolviert haben. Dieser Artikel hat ein Peer-Review-Verfahren durchlaufen. Nach Angaben der Autoren sind die Inhalte des Artikels produkt- und/oder dienstleistungsneutral, es bestehen keine Interessenkonflikte.
| Abkürzungsverzeichnis | |
| BVA | Berufsverband der Augenärzte Deutschlands |
| DMÖ | diabetisches Makulaödem |
| DRP | diabetische Retinopathie |
| DOG | Deutsche Ophthalmologische Gesellschaft |
| FDA | Food and Drug Administration, USA |
| IDF | International Diabetes Federation |
| IDx-DR | autonomes Diagnosesystem von IDx Technologies Inc., analysiert Fundusfotos mittels künstlicher Intelligenz |
| IVOM | intravitreale operative Medikamentenapplikation |
| LK oder LAKO | Laserkoagulation der Netzhaut |
| NPDRP | nicht-proliferative diabetische Retinopathie |
| OCT | Optische Kohärenztomographie |
| PDRP | proliferative diabetische Retinopathie |
| PPV | Pars-Plana-Vitrektomie: operative Entfernung des Glaskörpers zur Behandlung verschiedener Augenerkrankungen |
| PRN | pro re nata-Schema: IVOM-Injektionsschema, bei dem so lange Injektionen in Abständen von vier Wochen erfolgen, bis keine intraretinale Flüssigkeit mehr vorhanden ist. |
| PVR | proliferative Vitreoretinopathie: Augenerkrankung, die durch die Bildung von epiretinalen oder subretinalen Membranen gekennzeichnet ist. Gefahr der Netzhauttraktion und -ablösung. |
| T&E | Treat-and-Extend-Schema: IVOM-Injektionsschema, bei dem die Abstände zwischen den Sitzungen je nach Krankheitsaktivität angepasst und bei Therapieerfolg ausgeschlichen werden. |
| VEGF | Vascular Endothelial Growth Factor: Zelluläres Signalmolekül, das sowohl physiologisches als auch pathologisches Gefäßwachstum anregen kann. |